Estados Físicos da Matéria: Uma Abordagem Detalhada: Exemplo De Materiais Em Seus Estados Solido Fisico E Gasoso
Exemplo De Materiais Em Seus Estados Solido Fisico E Gasoso – A matéria, tudo o que ocupa espaço e possui massa, existe em diferentes estados físicos, sendo os mais comuns o sólido, o líquido e o gasoso. Compreender as propriedades e transições entre esses estados é fundamental para diversas áreas do conhecimento, desde a química e física até a engenharia e a medicina. A diferença entre esses estados reside na organização e interação das partículas que compõem a matéria – átomos, íons ou moléculas.
Estados Sólido, Líquido e Gasoso: Características e Transições
No estado sólido, as partículas estão fortemente unidas, resultando em uma forma e volume definidos. A transição para o estado líquido, chamada de fusão, ocorre com o aumento da temperatura, fornecendo energia suficiente para romper parte das ligações intermoleculares. No estado líquido, as partículas possuem maior mobilidade, mantendo um volume definido, mas adaptando-se à forma do recipiente. A vaporização, por sua vez, é a transição do líquido para o gasoso, onde as partículas se movem livremente, ocupando todo o volume disponível.
O processo inverso da vaporização é a condensação, e o inverso da fusão é a solidificação.
| Propriedade | Sólido | Líquido | Gasoso |
|---|---|---|---|
| Forma | Definitiva | Indefinida (adapta-se ao recipiente) | Indefinida (ocupa todo o volume disponível) |
| Volume | Definitivo | Definitivo | Indefinido (expansível) |
| Densidade | Alta | Intermediária | Baixa |
| Compressibilidade | Baixa | Baixa | Alta |
Materiais no Estado Sólido: Exemplos e Propriedades
Diversos materiais, com propriedades físicas e químicas distintas, existem no estado sólido. A estrutura cristalina, arranjo ordenado dos átomos, íons ou moléculas, influencia significativamente suas características.
- Ferro (Fe): Metal com alta resistência mecânica, usado na construção civil e na fabricação de aço.
- Diamante (C): Forma alotrópica do carbono, extremamente duro e com alto índice de refração, usado em joias e ferramentas de corte.
- Cloreto de Sódio (NaCl): Composto iônico, cristalino e solúvel em água, usado como sal de cozinha.
- Silício (Si): Semicondutor usado na fabricação de chips de computador.
- Gelo (H₂O): Forma sólida da água, menos densa que a água líquida, o que permite a flutuação do gelo na água.
O diamante e o cloreto de sódio apresentam estruturas cristalinas distintas. O diamante possui uma estrutura tetraédrica covalente, onde cada átomo de carbono está ligado a outros quatro átomos, formando uma rede tridimensional extremamente forte. Já o cloreto de sódio apresenta uma estrutura cúbica, com íons Na+ e Cl- alternados em uma rede iônica, mantidos unidos por forças eletrostáticas.
Materiais no Estado Líquido: Exemplos e Propriedades
Os líquidos, ao contrário dos sólidos, não possuem forma definida, adaptando-se ao recipiente que os contém. Propriedades como tensão superficial e viscosidade influenciam significativamente o seu comportamento.
| Líquido | Temperatura de Ebulição (°C) | Ponto de Fusão (°C) | Aplicações |
|---|---|---|---|
| Água (H₂O) | 100 | 0 | Solvente universal, consumo humano, indústria |
| Álcool Etílico (C₂H₅OH) | 78 | -114 | Solvente, desinfetante, combustível |
| Mercúrio (Hg) | 357 | -39 | Termômetros (uso em declínio devido à toxicidade), instrumentos científicos |
| Óleo de cozinha | Varia | Varia | Cozinhar, lubrificação |
| Sangue | 100 (aprox.) | 0 (aprox.) | Transporte de oxigênio e nutrientes no corpo humano |
A água apresenta alta tensão superficial devido às fortes ligações de hidrogênio entre suas moléculas. Já o álcool etílico possui menor tensão superficial. A viscosidade, resistência ao fluxo, também difere entre os líquidos, sendo a água menos viscosa que o óleo de cozinha.
Materiais no Estado Gasoso: Exemplos e Propriedades
Os gases são caracterizados por sua alta compressibilidade e expansibilidade, ocupando todo o volume disponível. A lei dos gases ideais descreve o comportamento de gases sob condições ideais, relacionando pressão (P), volume (V), quantidade de matéria (n) e temperatura (T): PV = nRT, onde R é a constante dos gases ideais.
O oxigênio e o dióxido de carbono são exemplos de gases com diferentes propriedades. O oxigênio é essencial para a respiração, enquanto o dióxido de carbono é um produto da respiração e um gás estufa. A compressibilidade do dióxido de carbono é maior que a do oxigênio em condições iguais de pressão e temperatura, devido às interações intermoleculares mais fortes presentes no CO₂.
Transições de Fase e Mudanças de Estado
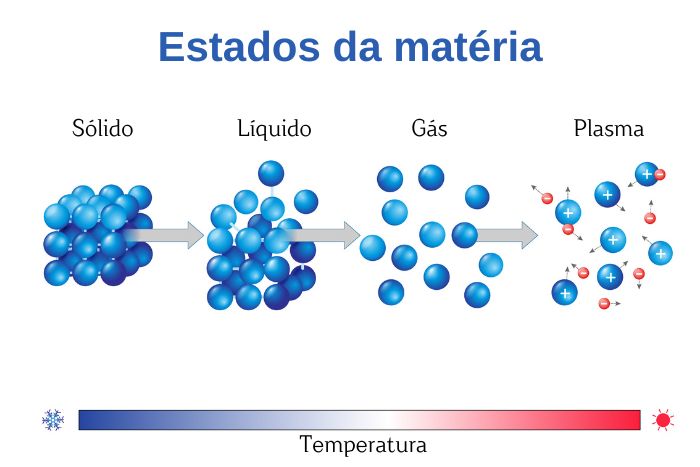
As mudanças de estado físico envolvem a absorção ou liberação de energia. A fusão (sólido para líquido), vaporização (líquido para gasoso) e sublimação (sólido para gasoso) requerem energia, enquanto a solidificação (líquido para sólido), condensação (gasoso para líquido) e deposição (gasoso para sólido) liberam energia. A água, por exemplo, sofre essas transições em temperaturas específicas, como 0°C (fusão/solidificação) e 100°C (vaporização/condensação) em pressão atmosférica.
Um diagrama de fases da água mostraria as regiões de pressão e temperatura onde a água existe como sólido, líquido ou gasoso, incluindo o ponto triplo (onde os três estados coexistem em equilíbrio) e o ponto crítico (acima do qual a distinção entre líquido e gás desaparece).
Aplicações Práticas dos Diferentes Estados Físicos, Exemplo De Materiais Em Seus Estados Solido Fisico E Gasoso
Os diferentes estados físicos da matéria possuem aplicações diversas em diversas áreas.
Aplicações de Sólidos na Indústria: O aço (estado sólido) na construção civil, o silício (estado sólido) na eletrônica e os polímeros (estado sólido) na fabricação de plásticos são exemplos de aplicações industriais de materiais no estado sólido.
Aplicações de Líquidos na Medicina: Soluções intravenosas (líquidos) para hidratação e medicamentos líquidos para administração oral ou injeção são exemplos de aplicações na medicina.
Aplicações de Gases na Agricultura: O dióxido de carbono (estado gasoso) é utilizado em estufas para estimular o crescimento das plantas.
De picos imponentes a gases invisíveis, a jornada pela matéria em seus estados sólido, líquido e gasoso nos revelou uma complexidade fascinante. Compreender as propriedades únicas de cada estado, as transições entre eles e suas inúmeras aplicações, é fundamental para avançar em diversas áreas do conhecimento e da tecnologia. Do design de materiais de alta resistência à utilização de gases em processos industriais, a ciência dos estados físicos da matéria molda nosso mundo de maneiras surpreendentes.
A exploração contínua deste tema promete desvendar ainda mais segredos e inspirar inovações que transformarão nosso futuro. Afinal, o conhecimento profundo da natureza da matéria é a chave para o progresso e a inovação.

